癌細胞選択的核酸医薬の創製
癌細胞選択的核酸医薬の創製
更新:2025/06/13
- 特徴・独自性
-
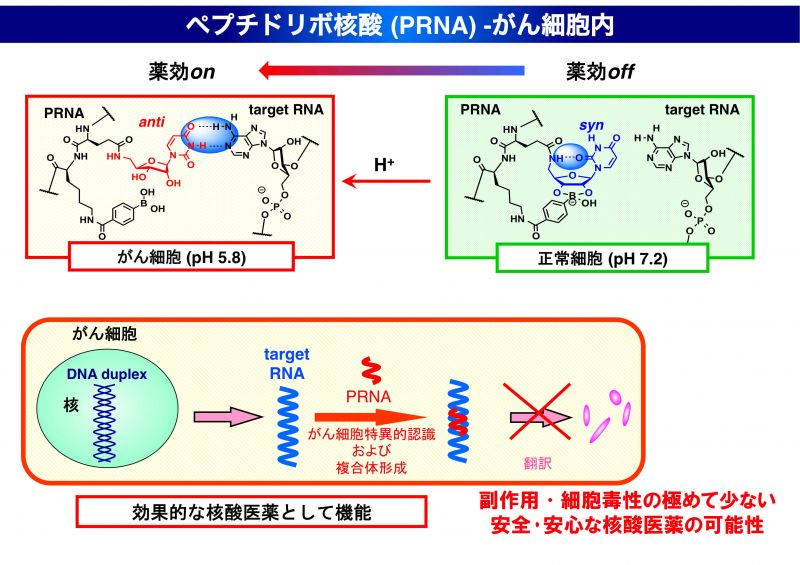
抗体医薬に次ぐ分子標的医薬として注目されている核酸医薬ですが、効果的な薬効発現と表裏一体的課題であるオフターゲット効果と呼ばれる副作用の低減がその実用化に向けた重要な解決すべき問題点として指摘されています。我々は従来の方法論とは全く異なる、標的がん細胞内でのみ薬効を発現し、正常細胞内では副作用を発現しない“ がん細胞選択的核酸医薬” という新しい研究戦略を提案し、その実現に向け研究を推進しています。具体的には増幅期のがん細胞に特徴的な低血流に基づく細胞内低酸素状態、ハイポキシアに注目し、ハイポキシアにより誘起される細胞内pH 低下をトリガーとした選択的薬効発現を実現する人工核酸創製に取り組み、核酸塩基の配向変化に基づく標的RNA 認識のOn-Off スイッチングを実現しました。現在、本学医学部 五十嵐教授、児玉教授らとの共同研究により、動物レベルの実証実験に取り組み、良好な初期的データを得ています。標的細胞選択的薬効発現という研究戦略は世界的にも類がなく、高い独自性を有しており、世界的に高く評価されています。
- 実用化イメージ
-
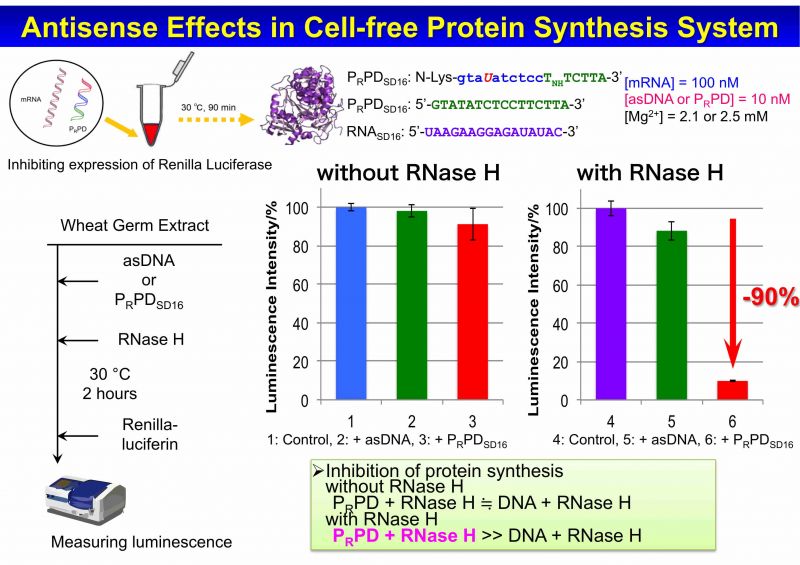
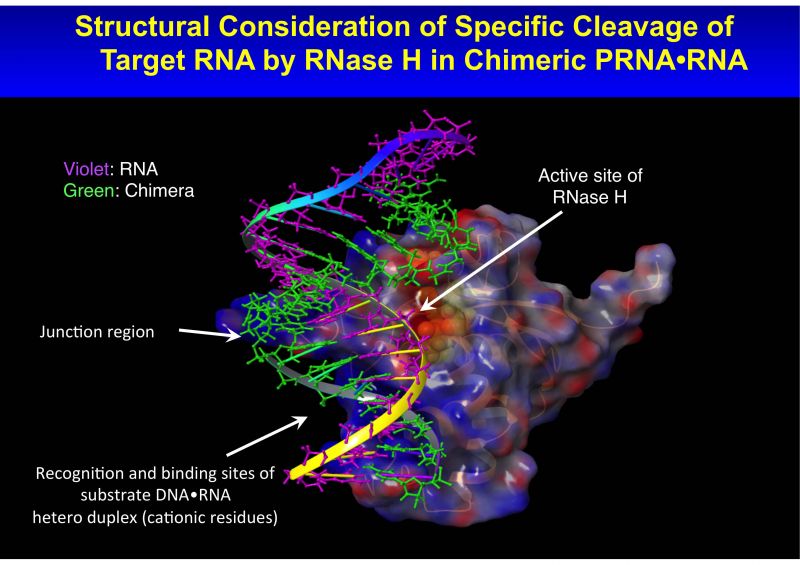
上記、がん細胞選択的核酸医薬創製の研究戦略の実用化を目指し、細胞内に導入可能な極低濃度の核酸医薬でも効果的な薬効発現を目指し、RNaseH を活用し、標的疾患細胞内で約1,000倍過剰に存在すると報告されている標的RNA を分解可能な触媒的核酸医薬法に適用可能なキメラ人工核酸(図3)開発に取組み、細胞レベルで有効性を実証し、動物試験に取組んでいます。
- キーワード


 ライフサイエンス
ライフサイエンス
 情報通信
情報通信
 環境
環境
 ナノテクノロジー・材料
ナノテクノロジー・材料
 エネルギー
エネルギー
 ものづくり・機械
ものづくり・機械
 社会基盤・安全
社会基盤・安全
 フロンティア・宇宙
フロンティア・宇宙
 人文・社会
人文・社会